Đối với một vắc-xin thương mại, bên cạnh các tiêu chí quan trọng như tính an toàn và hiệu quả bảo hộ cao, giá thành sản xuất hợp lý và tính tiện dụng trong quá trình sử dụng cũng là những yếu tố then chốt quyết định sự thành công của sản phẩm trên thực tế.
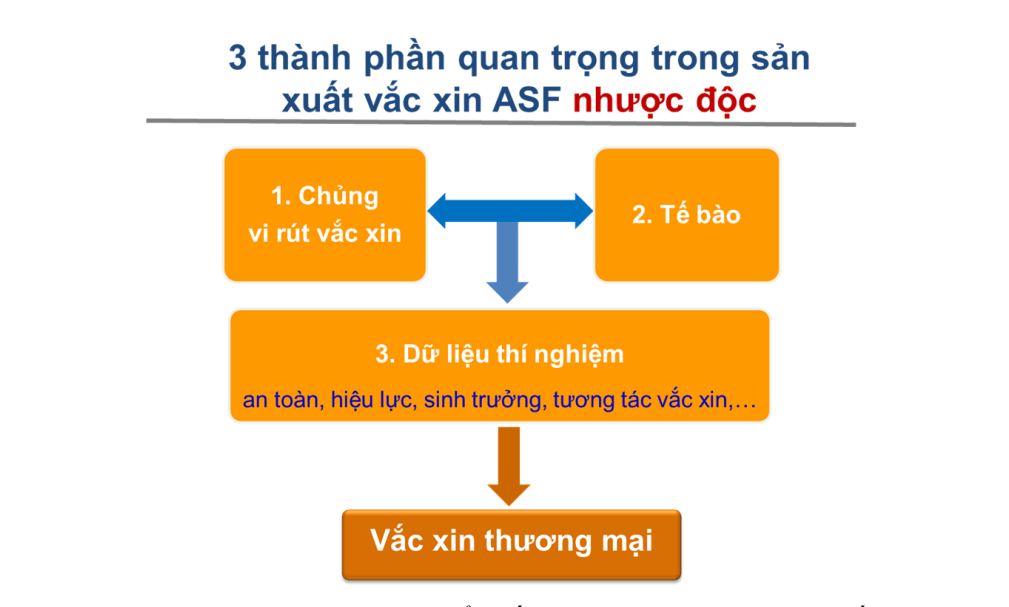
Trong số bảy nền tảng công nghệ được xem xét cho việc phát triển vắc-xin phòng bệnh ASF, công ty Avac, một trong những công ty đang thương mại hoá vaccine ASF, xác định vắc-xin sống nhược độc, phát triển bằng phương pháp cắt gen, là hướng đi khả thi nhất. Tuy nhiên, để có thể phát triển vắc-xin nhược độc trong thời gian ngắn nhất, cần đồng thời giải quyết ba thách thức kỹ thuật then chốt: (1) Lựa chọn và tối ưu hóa chủng vi-rút nhược độc có độ an toàn cao; (2) Phát triển được dòng tế bào liên tục cho phép vi-rút DTLCP nhân lên ổn định; (3) Xây dựng bộ dữ liệu toàn diện về đặc tính sinh học, tính sinh miễn dịch và độ an toàn của vắc-xin – đây là nền tảng khoa học thiết yếu để tiến tới sản xuất thương mại ở quy mô lớn.
Trong quá trình triển khai dự án, nhóm nghiên cứu tại Avac đã dần giải quyết được các rào cản trên như sau:
Chủng vi-rút vắc-xin
Từ 3 chủng vi-rút nhược độc được tạo ra bằng phướng pháp xóa gen được Hoa Kỳ chuyển giao, chúng tôi đã đánh giá lại đặc tính sinh học các ứng viên này, sau đó chọn ra một chủng virút rồi tiếp tục tối ưu. Chủng ASF-G-ΔMGF (mất 6 gene độc, thuộc hai họ gen MGF-360 và MGF505) được chúng tôi tiếp tục chọn lọc và cấy chuyển liên tục trên tế bào DMAC. Sau 30 đời cấy chuyển và chọn lọc, cloning, chúng tôi đã tạo ra một giống vi-rút gốc thỏa mãn các yêu cầu về vô trùng, tinh khiết, an toàn, bảo hộ cao đối với chủng vi-rút thực địa genotype II đang lưu hành chủ yếu tại Việt Nam. Kết quả giả trình tự toàn bộ genome của giống vi-rút vắc-xin (đã tải lên ngân hàng gen thế giới với accession number là PP529961) cho thấy giống vi-rút gốc của AVAC sở hữu một số đột biến khác biệt di truyền so với chủng ban đầu nhận từ Hoa Kỳ, tạo ra sự thay đổi cấu trúc trình tự ở 10 protein. Điều này lý giải cho việc virut đã nhược độc, an toàn hơn so với ứng viên ban đầu được chuyển giao. Từ giống vi-rút gốc (master seed) này, chúng tôi sản xuất ra các giống sản xuất (working seed) để sản xuất kháng nguyên cho các lô vắc-xin thương mại.
Tế bào dòng cho phép vi-rút ASF nhân lên ổn định
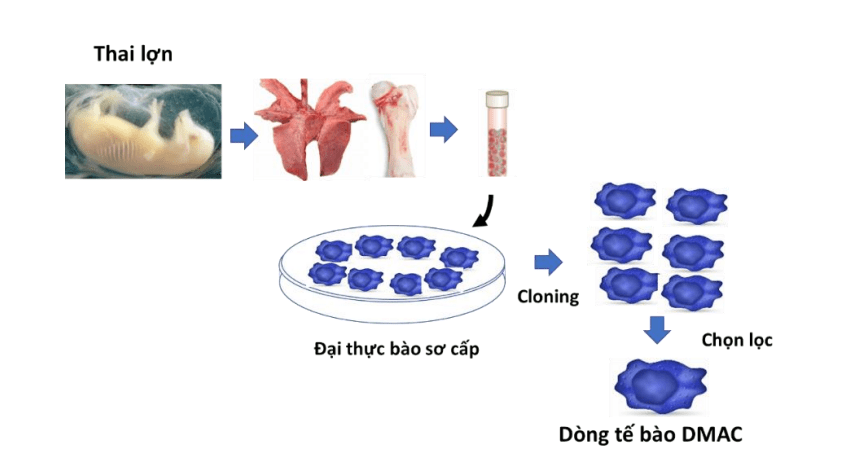
TS Nguyễn Văn Điệp đã phát triển một dòng tế bào có nguồn gốc từ đại thực bào tự nhiên, được phân lập từ phôi thai lợn. Dòng tế bào này có khả năng sinh trưởng liên tục, ổn định về đặc tính sinh học, không chứa các gen gây ung thư (thường được sử dụng để gây bất tử tế bào), không nhiễm các vi sinh vật ngoại lai, và có khả năng lưu trữ lâu dài ở nhiệt độ âm sâu. Đặc biệt, dòng tế bào này cho phép vi-rút vắc-xin DTLCP nhân lên nhanh chóng, đạt hiệu giá cao và ổn định về đặc tính sinh học. Dòng tế bào như vậy là thành phần cốt lõi trong quy trình kiểm soát chất lượng của từng lô vắc-xin sản xuất, đồng thời phù hợp với yêu cầu tăng sinh quy mô lớn trong sản xuất công nghiệp. Dòng tế bào này được đặt tên là DMAC (viết tắt của Diep’s Macrophage, đặt theo tên tác giả), và đã được đăng ký bảo hộ sáng chế tại Cục Sở hữu Trí tuệ.
Bộ dữ liệu toàn diện về đặc tính của vắc-xin thương mại
Để có một hướng dẫn sử dụng an toàn, hiệu quả cho người chăn nuôi, nhà quản lý thì thông tin đầy đủ, toàn diện về các khía cạnh khác nhau của một sản phẩm vắc-xin thương mại cần được hoàn thiện. Nhà sản xuất cần tiếp tục đánh giá các tiêu chí như tính ổn định về hiệu quả của sản phẩm, độ dài miễn dịch, tương tác với vắc-xin khác, khả năng truyền qua nhau thai, ảnh hưởng của miễn dịch mẹ truyền, quy trình tiêm vắc-xin theo lứa tuổi, ảnh hưởng đến năng suất trong điều kiện tình trạng sức khỏe đàn lợn khác nhau, khả năng bài thải và truyền ngang trong điều kiện chăn nuôi thực tế, sự tồn dư vi rút trong thân thịt và nội tạng, khả năng phân biệt chủng vi-rút vắc-xin với chủng vi-rút thực địa, …
Để có đủ dữ liệu, nhà sản xuất cần tiếp tục làm rất nhiều thử nghiệm trong phòng thí nghiệm và trên động vật, tại các cơ sở chăn nuôi. Mỗi thử nghiệm cần được tính toán, thiết kế phù hợp, khoa học, dựa trên các tiêu chuẩn hiện hành với vắc-xin sống nói chung và với vắc-xin DTLCP nói riêng. Đặc biệt trong hoàn cảnh chưa có một tiêu chuẩn quốc tế nào cho vắc-xin DTLCP được đưa ra, công ty AVAC phải tự thiết kế các tiêu chuẩn, đồng thời tích hợp cao nhất các tiêu chuẩn trong dự thảo mới nhất do Tổ chức Thú y thế giới (WOAH) đang xây dựng. Sau hơn 100 thử nghiệm trên động vật được thực hiện với các kết quả tích cực, AVAC đã có bộ dữ liệu cơ bản về nhiều tiêu chí của sản phẩm, để tự tin đưa ra khuyến cáo sử dụng cho từng đối tượng.
Kết quả nghiên cứu
Kết quả nghiên cứu cho thấy, với liều bảo hộ tối thiểu khi chứa 103 vi-rút nhược độc ASFG-ΔMGF, chủng vắc-xin an toàn cho lợn thịt từ 4 tuần tuổi trở lên; vắc-xin tạo miễn dịch bảo vệ nhanh sau 2 tuần, và bảo vệ cao nhất sau 4 tuần; tỷ lệ bảo hộ cao > 90% lợn tiêm vắc xin; thời gian bảo hộ có thể kéo dài trên 5 tháng; vắc-xin không ảnh hưởng tới khả năng tăng trưởng của lợn; không ảnh hưởng đáp ứng miễn dịch của vắc-xin khác. Nghiên cứu ban đầu cũng cho thấy chủng vắc-xin an toàn và bảo hộ tốt cho lợn nái và đực giống.

“Từ kết quả nghiên cứu trên, công ty AVAC đã đăng ký xin cấp phép lưu hành vắc-xin sử dụng phòng bệnh DTLCP cho lợn thịt, với tên thương mại là Avac ASF Live. Vắc-xin được khuyến cáo sử dụng cho lợn thịt từ 4 tuần tuổi trở lên, chỉ cần tiêm 1 mũi duy nhất, đã có thể tạo miễn dịch bảo hộ kéo dài tới 5 tháng, đủ bảo vệ toàn bộ vòng đời lợn thương phẩm. Với quy trình tiêm 1 mũi cho lợn từ 4 tuần tuổi (sau cai sữa), vắc-xin AVAC ASF LIVE thể hiện tính tiện dụng.”
Đăng ký và thương mại hóa sản phẩm vắc-xin AVAC ASF LIVE
Vắc-xin AVAC ASF LIVE đã trải qua quá trình kiểm định nghiêm ngặt và kỹ lưỡng trước khi được cấp phép lưu hành. Cục Thú y đã tiến hành đánh giá chủng giống, kiểm nghiệm 3 lô vắc-xin và khảo nghiệm an toàn, hiệu quả ở hai trang trại theo quy trình chặt chẽ đã được phê duyệt. Sau đó, Cục Thú y cũng đánh giá tính an toàn và hiệu quả bảo hộ khi sử dụng vắc-xin AVAC ASF LIVE ở 4 trang trại ở Bắc Giang và Hà Nội, với quy mô nuôi từ 500 – 20.000 lợn thịt. Kết quả cho thấy vắc-xin AVAC ASF LIVE an toàn cho lợn ở nhiều lứa tuổi (4-13 tuần tuổi), ngay cả khi tiêm quá liều (10 liều), và tỷ lệ bảo hộ đạt trung bình trên 80% khi công cường độc với chủng vi-rút thực địa genotype II phân lập tại Việt Nam. Ngày 8.7.2022, vắc-xin AVAC ASF LIVE được cấp phép lưu hành có kiểm soát tại Việt Nam. Sau khi phối hợp với các cơ quan chức năng, chuyên ngành đánh giá tính an toàn, hiệu quả của vắc-xin ở quy mô trên 600.000 liều tại gần 600 trang trại, vắc-xin AVAC ASF LIVE đã được cho phép lưu hành rộng rãi và xuất khẩu từ ngày 24/7/2023. Đây là vắc-xin DTLCP đầu tiên được chính phủ cho phép thương mại toàn quốc và xuất khẩu.

Sau khi được lưu hành, công ty AVAC đã tiếp tục phối hợp thực hiện thêm các thử nghiệm tại hơn 20 tỉnh thành với quy mô từ 100-3000 lợn thịt tại hàng trăm cơ sở chăn nuôi. Vắc-xin chứng minh tính an toàn và hiệu quả bảo hộ khi đưa vào sử dụng thực tế.
Đến nay, nhiều doanh nghiệp chăn nuôi lớn đã triển khai sử dụng vắc-xin. Đồng thời, nhiều địa phương như Cao Bằng, Lạng Sơn, Lai Châu, Sơn La, Bắc Ninh, Hải Dương, Hải Phòng, Quảng Ngãi, Trà Vinh v.v. cũng đã tổ chức tiêm phòng đại trà cho đàn lợn. Tính đến đầu năm 2025, công ty AVAC đã cung cấp khoảng 2,5 triệu liều vắc-xin cho thị trường trong nước. Riêng các chi cục Chăn cuôi Thú y và Trung tâm dịch vụ Nông nghiệp các tỉnh, công ty AVAC đã phân phối trên 600.000 liều cho các đơn vị này.
Không chỉ giới hạn trong phạm vi Việt Nam, vắc-xin AVAC ASF LIVE được giới thiệu, chia sẻ tại nhiều diễn đàn khoa học quốc tế uy tín chủ trì bởi các tổ chức hàng đầu thế giới, như Liên minh Toàn cầu về Dịch tả lợn châu Phi (GARA), Tổ chức Nông Lương Liên Hợp Quốc (FAO), Tổ chức Thú y Thế giới (WOAH), Viện Chăn nuôi Quốc tế (ILRI), Hiệp hội Bệnh lợn Philippines, Hiệp hội Đậu nành Hoa Kỳ (USSEC), cũng như các trường đại học.
Song song với các đánh giá tại Việt Nam, từ tháng 2/2023, Cục Chăn nuôi Thú y (BAI) Philippines tiến hành các thử nghiệm vắc-xin AVAC ASF LIVE trong quy mô phòng thí nghiệm và 10 trang trại. Kết quả đánh giá cho thấy vắc-xin AVAC ASF LIVE an toàn và kích thích sinh miễn dịch cao trên đàn lợn. Chính phủ Philippines cho phép Bộ Nông nghiệp Philippines nhập vắc-xin AVAC ASF LIVE và sử dụng. Đây là quốc gia đầu tiên ngoài Việt Nam chính thức cấp phép sử dụng vắc-xin vào tháng 7/2024, với 460.000 liều đã được nhập khẩu. Ngoài ra, Nigeria cũng đã nhập 5.000 liều để phục vụ cho việc thử nghiệm và đăng ký lưu hành. Việc đánh giá và đăng lý lưu hành đang được triển khai ở các quốc gia khác như Nepal, Ấn Độ, Malaysia, Myanmar, Campuchi, Tanzania, Ukraine, Serbia, Sri Lanka…
Thách thức và giải pháp trong tương lai
Trong quá trình lưu hành, mầm bệnh liên tục biến đổi đặc tính sinh học, tiến hóa độc lực, làm thay đổi tính kháng nguyên và do đó hiệu quả của vắc-xin bị ảnh hưởng. Do đó, mỗi vắc-xin đều có những vòng đời nhất định, vòng đời dài hay ngắn phụ thuộc chủ yếu vào dịch tễ bệnh và công nghệ sử dụng. Thực tế cho thấy vi-rút DTLCP biến đổi nhanh chóng với nhiều biến thể đã được báo cáo tại Việt Nam.
Đặc biệt, từ năm 2021, chủng tái tổ hợp giữa genotype I và II lần đầu được báo cáo tại Trung Quốc, sau đó lây lan sang Việt Nam và Mông Cổ, Nga. Điều nguy hiểm là các vắc-xin thương mại hiện có tại Việt Nam, hay các ứng viên vắc-xin ở Trung Quốc không thể bảo hộ lợn chống lại biến chủng này. Điều này cho thấy một thách thức mới xuất hiện, và trong tương lai, biến chủng mới này có thể lan rộng, đòi hỏi sẽ cần có một vắc-xin với phổ bảo hộ rộng hơn, bao gồm cả chủng tái tổ hợp này. Đứng trước những thách thức đó, là một đơn vị nghiên cứu và phát triển vắc-xin, AVAC đã và đang chủ động tiếp cận, hợp tác với các đơn vị nghiên cứu, làm chủ các công nghệ hiện đại để nhanh chóng tạo ra các ứng viên vắc-xin, chuẩn bị giải pháp cho thế hệ vắc-xin DTLCP tiếp theo.
Ngoài ra, việc sử dụng vắc-xin cho lợn giống (bao gồm nái và đực giống) là yêu cầu cấp thiết nhằm tăng cường khả năng bảo hộ cho mọi đối tượng trong quần thể lợn, đảm bảo miễn dịch đàn. Nhận thức rõ tầm quan trọng này, Công ty AVAC đã kiên trì đánh giá và tối ưu sản phẩm cùng quy trình sản xuất, nhằm đảm bảo vắc-xin AVAC ASF LIVE hiện đang lưu hành có thể sử dụng an toàn và hiệu quả cho mọi đối tượng lợn, bao gồm cả lợn giống. Năm 2024, AVAC đã phối hợp với Trung tâm Kiểm nghiệm thuốc Thú y Trung ương I và Cục Chăn nuôi – Thú y xây dựng bộ tiêu chuẩn đánh giá vắc-xin phòng Dịch tả lợn châu Phi (DTLCP) dành cho lợn giống. Đây là cơ sở quan trọng để Cục Chăn nuôi – Thú y tiếp tục triển khai đánh giá và tiến tới cấp phép chính thức cho việc sử dụng vắc-xin AVAC ASF LIVE trên lợn giống tại Việt Nam trong thời gian tới.
Trích lược bài viết của Tiến sĩ Nguyễn Văn Điệp, Tổng giám đốc Công ty Cổ phần AVAC Việt Nam

Leave a comment